首页 >
行业动态 > 【COF载药】:一种用于比率型缺氧成像和氧剥夺条件下药物活性增强的光激活诊疗组合
【COF载药】:一种用于比率型缺氧成像和氧剥夺条件下药物活性增强的光激活诊疗组合
摘要复述:
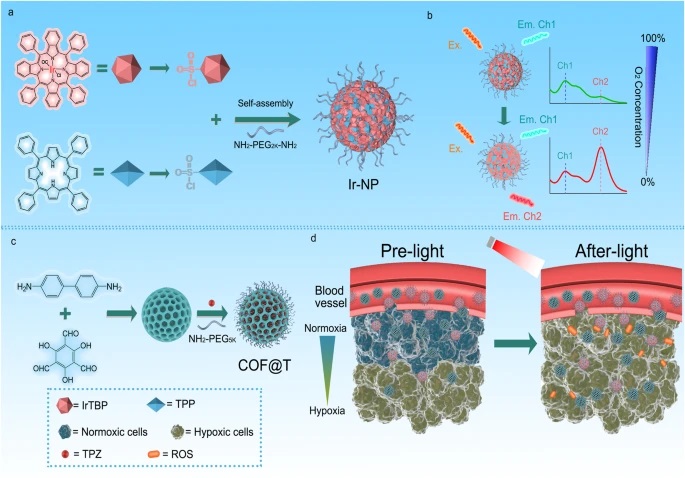
南京大学蒋锡群老师等报道的本篇文章中(Nat Commun 15, 153 (2024) )设计了一种用于光激活的比率型缺氧成像、缺氧调控和前药激活的诊疗组合。该组合包括一种氧敏感的近红外发射比率型磷光探针和一种负载缺氧激活前药的共价有机框架。在该组合中,探针发挥了两个作用:通过比率成像定量监测氧浓度,以及通过光动力治疗消耗肿瘤的氧。同时,增强的肿瘤缺氧微环境可以提高共价有机框架中负载的前药的细胞毒性,从而提高体内抗肿瘤治疗效果。该诊疗组合可以根据实时肿瘤缺氧水平精确提供治疗方案并筛选缺氧激活前药,为开发以缺氧靶向前药为基础的缺氧介导肿瘤诊疗提供了一种策略。
研究背景:
(1) 缺氧是肿瘤微环境的一个标志性特征,在肿瘤发生、进展、转移和对常规及靶向癌症治疗的耐药中起关键作用。
(2) 已开发了一系列缺氧响应性诊疗系统,通常由两个关键组分组成:用于成像检测缺氧的荧光探针和用于治疗的治疗剂。但大多数缺氧响应性探针仍处于定性阶段,缺乏定量能力,而治疗剂在低氧环境下疗效较低。
(3) 本文作者提出了一种新的诊疗组合策略,将定量缺氧报告和缺氧激活前药结合起来,通过选择有利的药物和治疗方案,根据肿瘤缺氧调节产生最大的治疗反应。
实验部分:
(1) 合成了一种氧敏感的近红外发射比率型磷光纳米探针(Ir-NP),实现了组织氧浓度的定量检测。
(2) 制备了一种由苯二胺和三甲酰基三羟基苯制成的共价有机框架(COF),并负载了缺氧激活前药替拉扎明(TPZ)。
(3) 将Ir-NP和COF@TPZ组合,Ir-NP在650nm光照下产生活性氧物种,消耗肿瘤氧,增强COF@TPZ的缺氧细胞毒性。
(4) 该诊疗组合在体内显著抑制肿瘤生长。将该方法拓展到其他缺氧激活前药如AQ4N、PR104、TH-302等,均取得了良好的抗肿瘤效果。
分析测试:
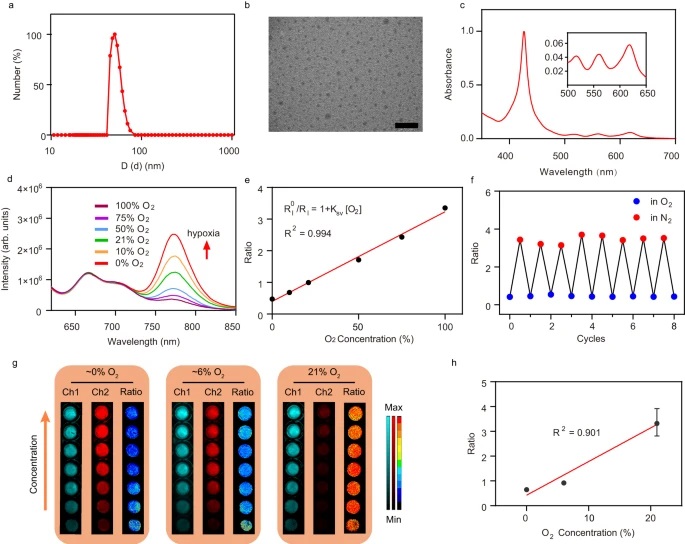
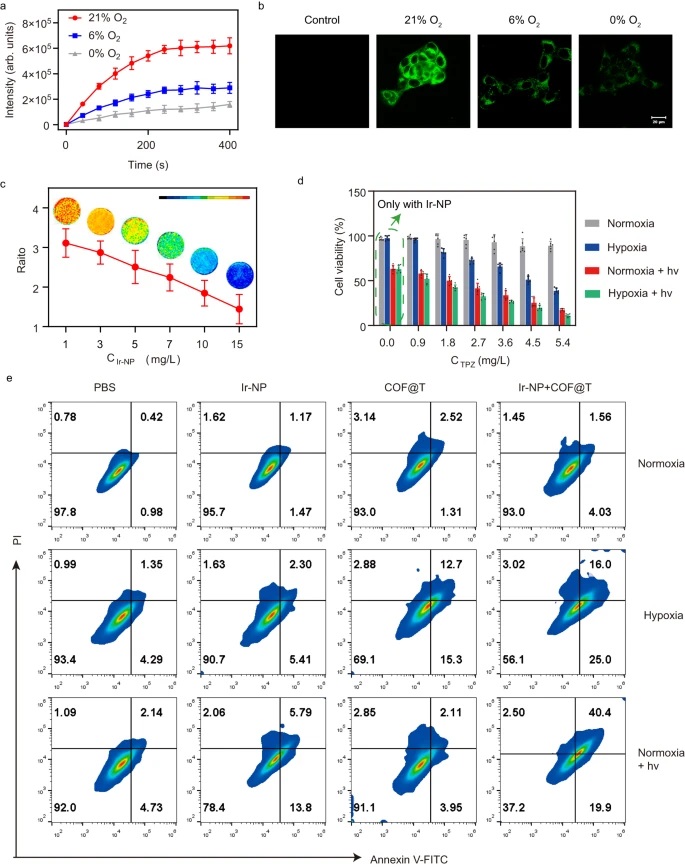
(1) Ir-NP的流体动力学直径约为50nm,比表面积为580.42 m2/g,孔径为2.4nm。不同氧浓度下,Ir-NP在774nm处的磷光发射强度与氧浓度呈线性相关(R2=0.994)。
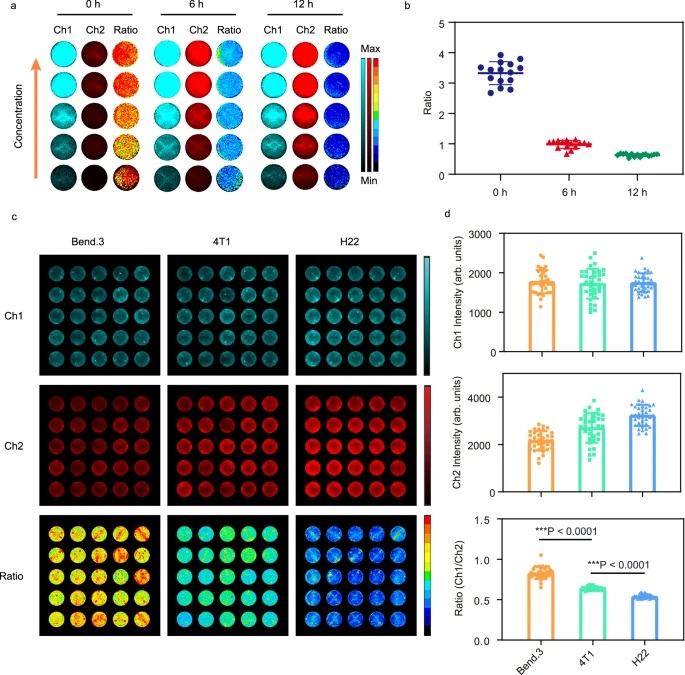
(2) 细胞实验表明,Ir-NP可定量检测不同细胞系的氧消耗率,正常细胞Bend.3氧消耗最低,肿瘤细胞4T1和H22氧消耗较高。
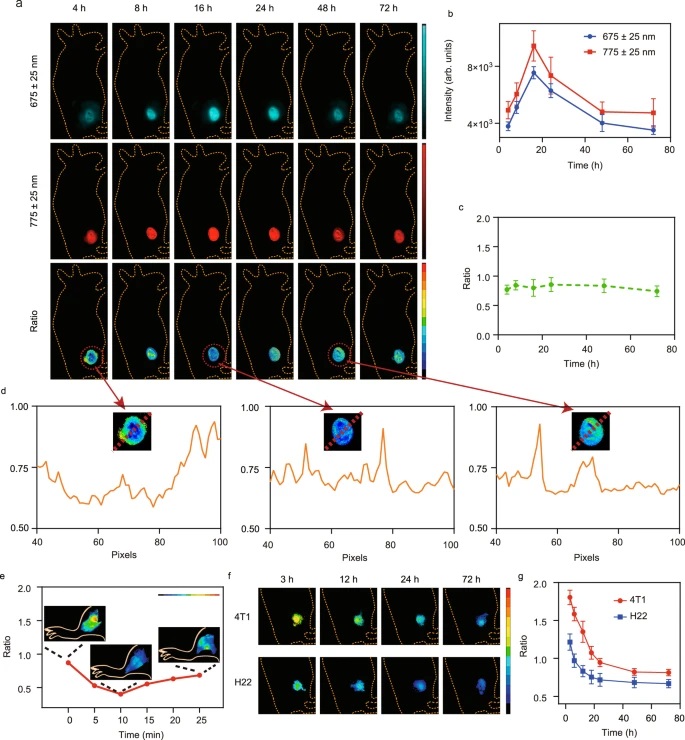
(3) 动物实验显示,Ir-NP可实时定量监测肿瘤组织的氧浓度,捕捉到肿瘤内显著的氧浓度空间异质性,并对血流限制引起的肿瘤缺氧变化做出快速响应。
(4) 650nm光照下,Ir-NP可有效产生单线态氧。低氧浓度下COF@TPZ的细胞毒性明显高于常氧条件。
结论总结:
(1) 本文构建了一种光激活的具有比率成像和组织氧调节功能以及缺氧激活前药的诊疗组合。
(2) 该诊疗组合不仅可以通过比率NIR成像定量监测肿瘤缺氧水平,还可以调节肿瘤缺氧程度,为选择有利药物和治疗方案提供指导,发挥缺氧激活前药的最大治疗效率。
(3) 该研究为开发基于缺氧靶向前药的缺氧介导肿瘤诊疗提供了一种策略。未来可进一步探索灵敏度和特异性更高的探针,扩大缺氧特异性前药的种类,为个性化癌症治疗提供更多选择。

展望与建议:
(1) 文章主要关注了治疗效果的研究,对诊断成像的定量性及准确性的评估还不够深入,建议补充更多实验数据支撑Ir-NP比率成像定量缺氧的能力。
(2) COF材料的生物相容性和代谢过程有待进一步考察,以确保其临床应用的安全性。
(3) 目前研究仅局限于皮下肿瘤模型,建议后续开展原位肿瘤模型的研究,以更好地模拟人体内肿瘤微环境。
(4) 可进一步优化给药剂量和时间,并评估长期治疗效果及毒副作用。
(5) 建议深入机制研究,阐明Ir-NP和COF@TPZ协同增敏的分子机制,为临床转化提供理论基础。
A light-activatable theranostic combination for ratiometric hypoxia imaging and oxygen-deprived drug activity enhancement
文章作者:Lei Ge, Yikai Tang, Chongzhi Wang, Jian Chen, Hui Mao & Xiqun Jiang
DOI:10.1038/s41467-023-44429-y
文章链接:https://doi.org/10.1038/s41467-023-44429-y





