首页 >
行业动态 > 【卟啉COF-PDT疗法】具有交错I/II型基序的强共价有机框架纳米光敏剂用于缺氧肿瘤的光动力免疫治疗
【卟啉COF-PDT疗法】具有交错I/II型基序的强共价有机框架纳米光敏剂用于缺氧肿瘤的光动力免疫治疗
摘要:
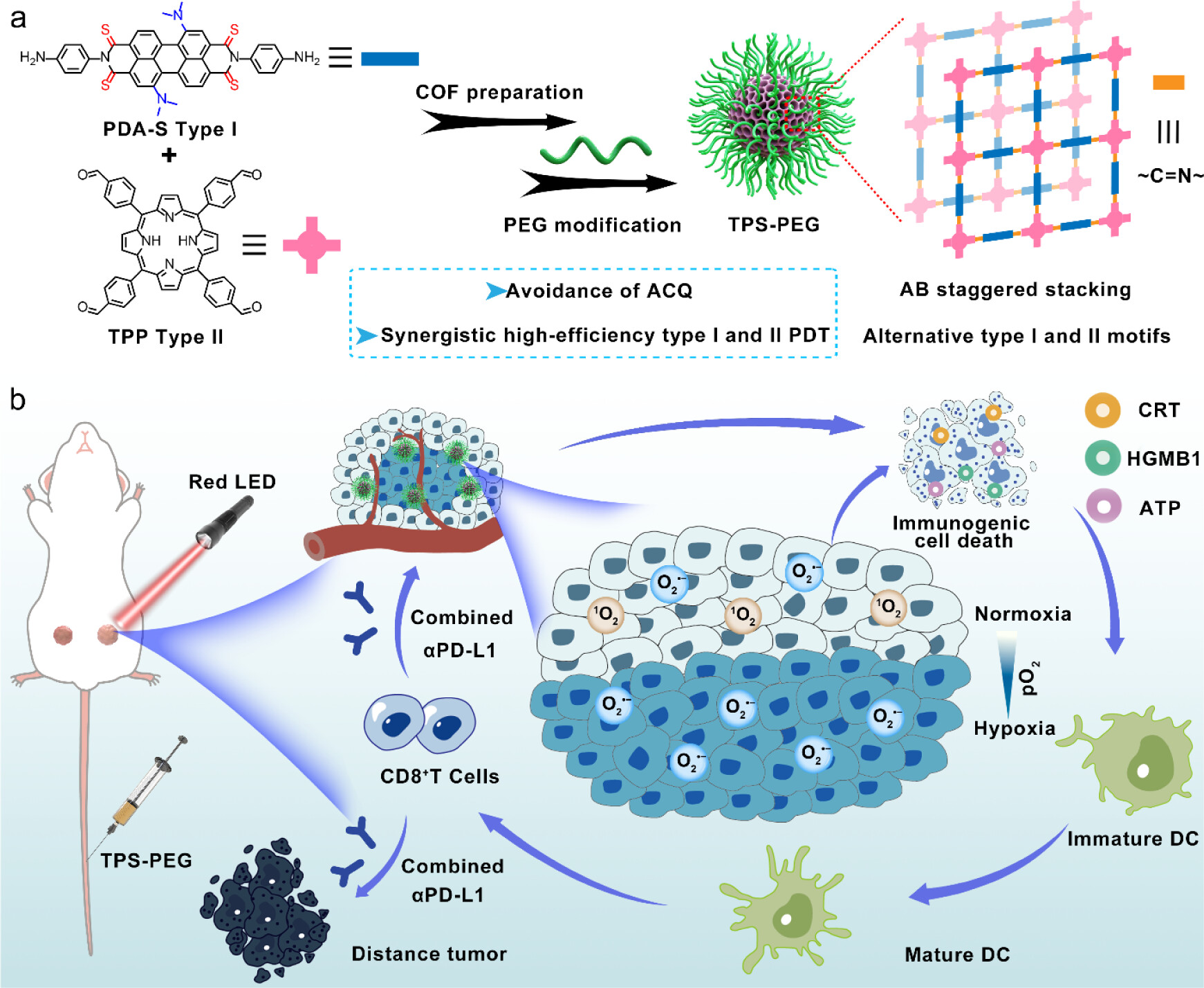
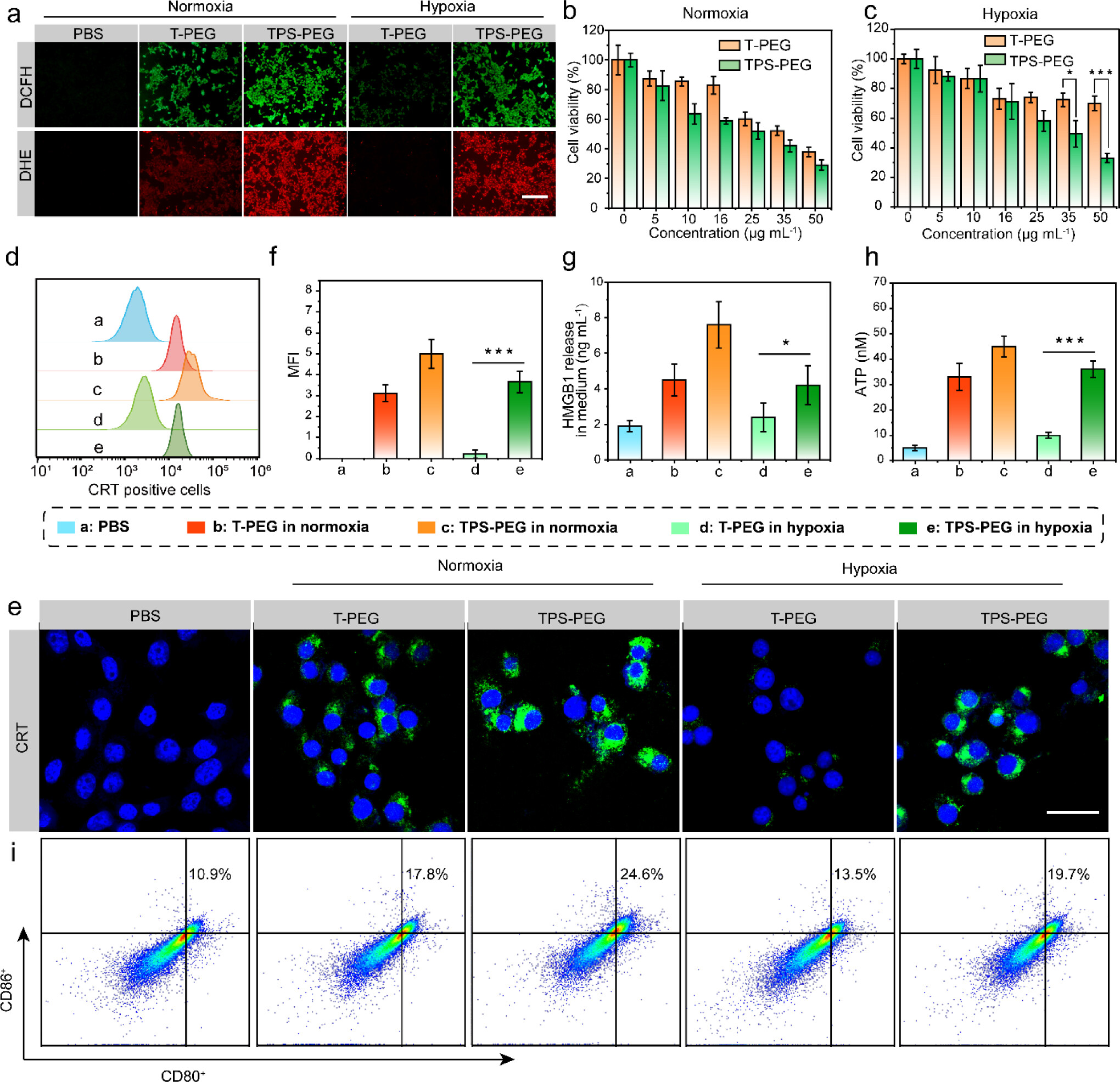
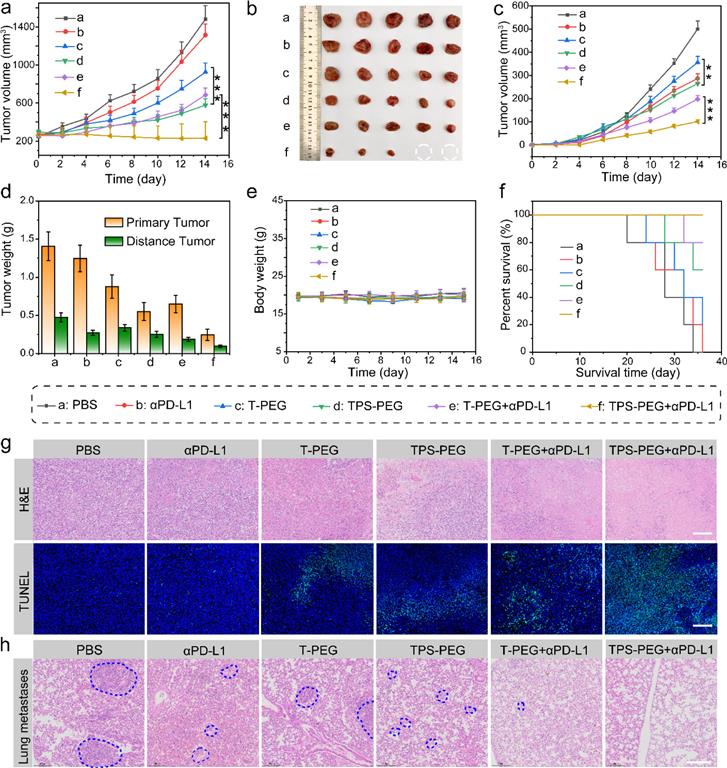
西安交通大学葛治伸老师等报道的本篇文章(ACS Nano 2024)中介绍了一种新型的共价有机框架(COF)纳米光敏剂,该光敏剂结合了I型和II型光动力治疗(PDT)的特点,以克服实体瘤乏氧微环境对治疗效果的限制。通过分子内供体-受体结合和硫取代,制备了高效的I型光敏剂,并与II型光敏剂反应形成COF纳米光敏剂,其在层内交替排列I型和II型光敏剂模式,并在层间形成交错的AB堆叠,以避免聚集引起的猝灭(ACQ)。该纳米光敏剂在光照下能有效产生单线态氧(1O2)和超氧阴离子自由基(O2•−),在乏氧条件下也能持续产生大量O2•−。这种强大的活性氧(ROS)生成能力导致了高效的细胞凋亡和免疫原性细胞死亡(ICD),与免疫检查点抑制剂联合使用时,能有效地消除大块乏氧原发肿瘤并抑制转移,通过光动力免疫治疗发挥作用。
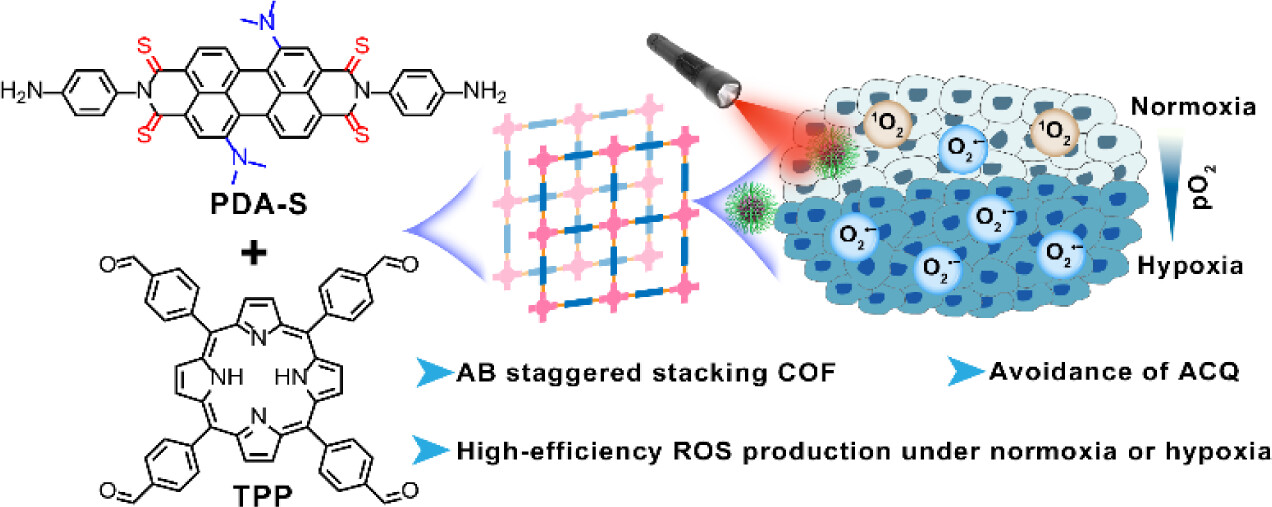
研究背景:
1)光动力治疗(PDT)是一种有前景的癌症治疗手段,但其在实体瘤治疗中受到乏氧微环境的限制,尤其是依赖氧气产生ROS的II型PDT。
2)已有研究通过提供氧气或原位产生氧气来提高肿瘤内的氧气水平,以及将I型和II型PDT效果整合到一个系统中。
3)作者设计了一种基于Perylene衍生物的I型光敏剂,通过分子内供体-受体结合和硫取代来增强ISC能力和电子转移能力,制备了具有交错堆叠结构的COF纳米光敏剂,有效避免了ACQ,并提高了ROS产生效率。
实验部分:
1. 光敏剂PD-Boc的合成:
1) 将1,7-二溴-3,4,9,10-Perylene四羧酸二酐(15.4 g, 28 mmol)和tert-butyl (4-aminophenyl) carbamate(11.6 g, 56 mmol)溶解于无水DMF(300 mL)中。
2) 将混合物的温度缓慢升至130°C,并保持24小时反应。
3) 将反应后的圆底烧瓶置于室温下自然冷却,然后将反应液滴加到乙醚中进行沉淀,通过过滤移除溶剂得到深红色的固体。
4) 粗固体通过硅胶柱色谱(使用DCM中0%至2%甲醇作为洗脱液)纯化,得到深红色的PD-Boc固体产品(16.9 g, 产率65%)。
2. 光敏剂PD-Boc-DA的合成:
1) 将PD-Boc分子(16 g, 17.24 mmol)和CuBr(43 mg, 0.3 mmol)加入DMF(300 mL)中。
2) 将40%的水溶液二甲基胺(19.4 g)滴加到反应体系中,在60°C下反应24小时。
3) 反应完成后,将混合溶液滴加到乙醚中进行沉淀,过滤并用甲醇洗涤,通过硅胶柱色谱(使用DCM中0%至2.5%甲醇作为洗脱液)纯化,得到最终的黑绿色PD-Boc-DA产品(7.3 g, 产率49%)。
3. 光敏剂PDA的合成:
1) 将PD-Boc-DA(7.3 g, 8.5 mmol)悬浮在DCM(400 mL)中。
2) 滴加CF3COOH(300 mL)并在室温下反应6小时。
3) 当pH值达到8-9时,滴加1M的NaOH溶液,随后使用DCM(300 mL)三次提取溶液。
4) 有机层溶液经过无水Na2SO4干燥,并在真空中浓缩,得到深绿色的PDA产品(4.4 g, 产率80%)。
4. 光敏剂PDA-S的合成:
1) 将PDA(4 g, 6.08 mmol)和Lawson's试剂(14.8 g, 36.4 mmol)在氮气保护下引入无水甲苯(300 mL)中,并加热至120°C回流24小时。
2) 混合物冷却至室温后,滴加到乙醚中进行沉淀,过滤并用甲醇洗涤。
3) 粗产品通过柱色谱(使用DCM/甲醇95:5,v/v作为洗脱液)纯化,得到黑色固体PDA-S(1.58 g, 产率36%)。
分析测试:
1. 核磁共振(NMR)分析:使用Bruker AV400 NMR 400MHz谱仪记录所有1H NMR谱图,使用DMSO-d6作为溶剂。
2. 粒径和粒径分布:使用带有Malvern Zeta大小Nano ZS90的动态激光光散射(DLS)装置测量。
3. 紫外-可见(UV-vis)光谱:使用UV-2401PC UV-可见分光光度计(Sahimadzu)测试。
4. 荧光光谱:使用F-4600荧光分光光度计(Hitachi)测试。
5. 傅里叶变换红外(FTIR)光谱:在Nicolet 8700 Fourier变换红外光谱仪上测试。
6. 电子顺磁共振(ESR)信号:使用Bruker E500仪器记录。
7. 材料微观结构:使用高分辨率透射电子显微镜(HR-TEM, Talos F200X, 美国)、场发射扫描电子显微镜(SEM, GeminiSEM 500, 德国)和X射线衍射(XRD, X'Pert MPD, 荷兰)表征。
8. X射线光电子能谱(XPS):使用ESCALAB250 Xi仪器(Thermo Fisher Scientific, 英国)进行。
9. 高效液相色谱(HPLC)分析:在Shimadzu HPLC系统上进行,配备LC-20AP二元泵、C18柱和SPD-20A UV-Vis检测器。
10. 荧光显微镜成像:使用OLYMPUS X71进行荧光成像。
11. 共聚焦激光扫描显微镜(CLSM):使用Leica TCS SP5显微镜进行CLSM图像观察。
12. 活体分布和积累研究:使用Xenogen IVIS spectrum光学成像设备研究样品在体内的分布和积累。
总结:
本文成功设计并制备了一种新型COF纳米光敏剂,该光敏剂结合了I型和II型PDT的特点,通过分子内供体-受体结合和硫取代增强了ISC能力和电子转移能力。COF结构的设计有效避免了ACQ,提高了ROS的产生效率。在体内外实验中,TPS-PEG展现了优异的肿瘤积累、ROS生成能力和光动力治疗效果,能够有效诱导ICD,逆转肿瘤免疫抑制微环境,并与免疫检查点抑制剂联合使用时,显著提高了治疗效果。
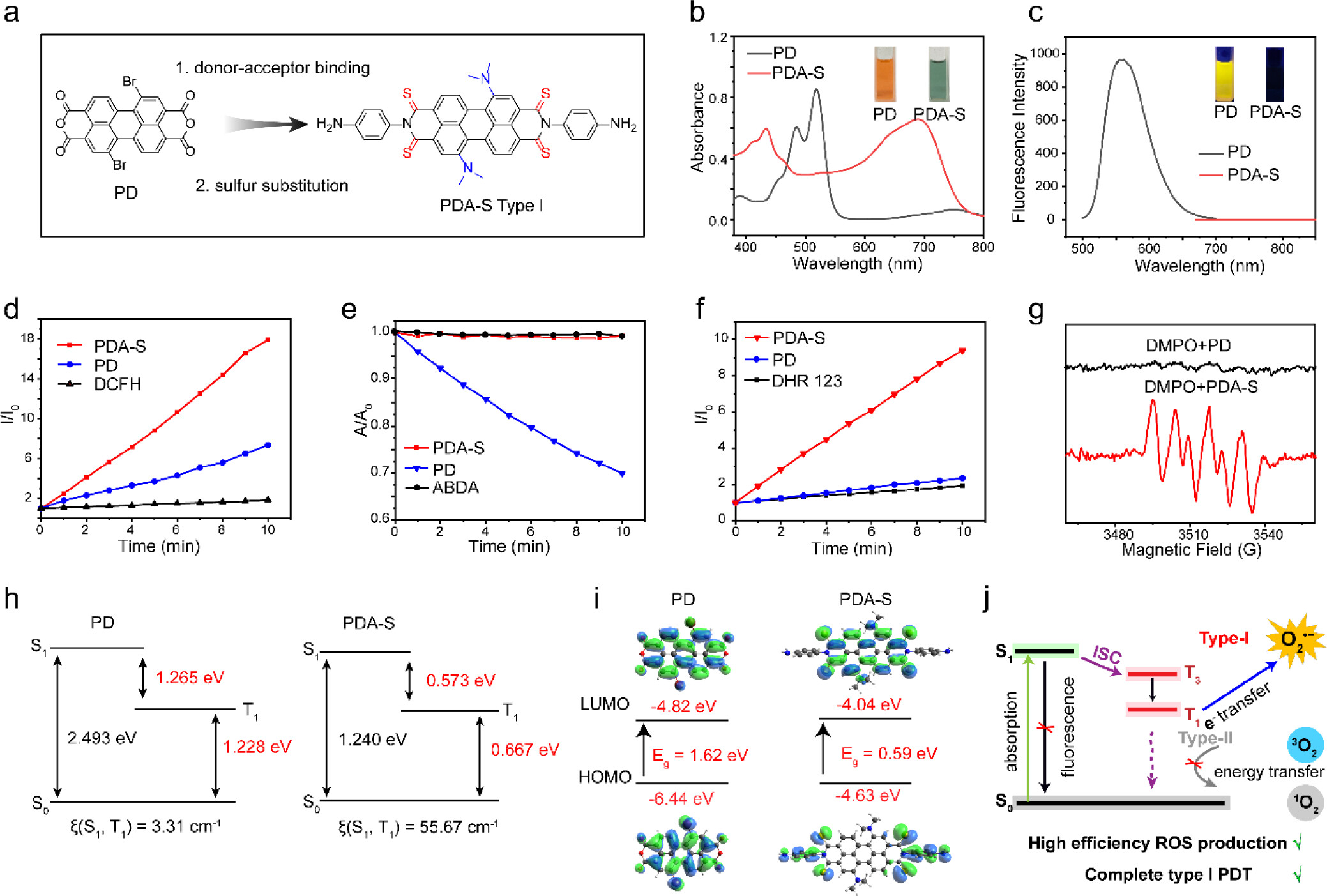
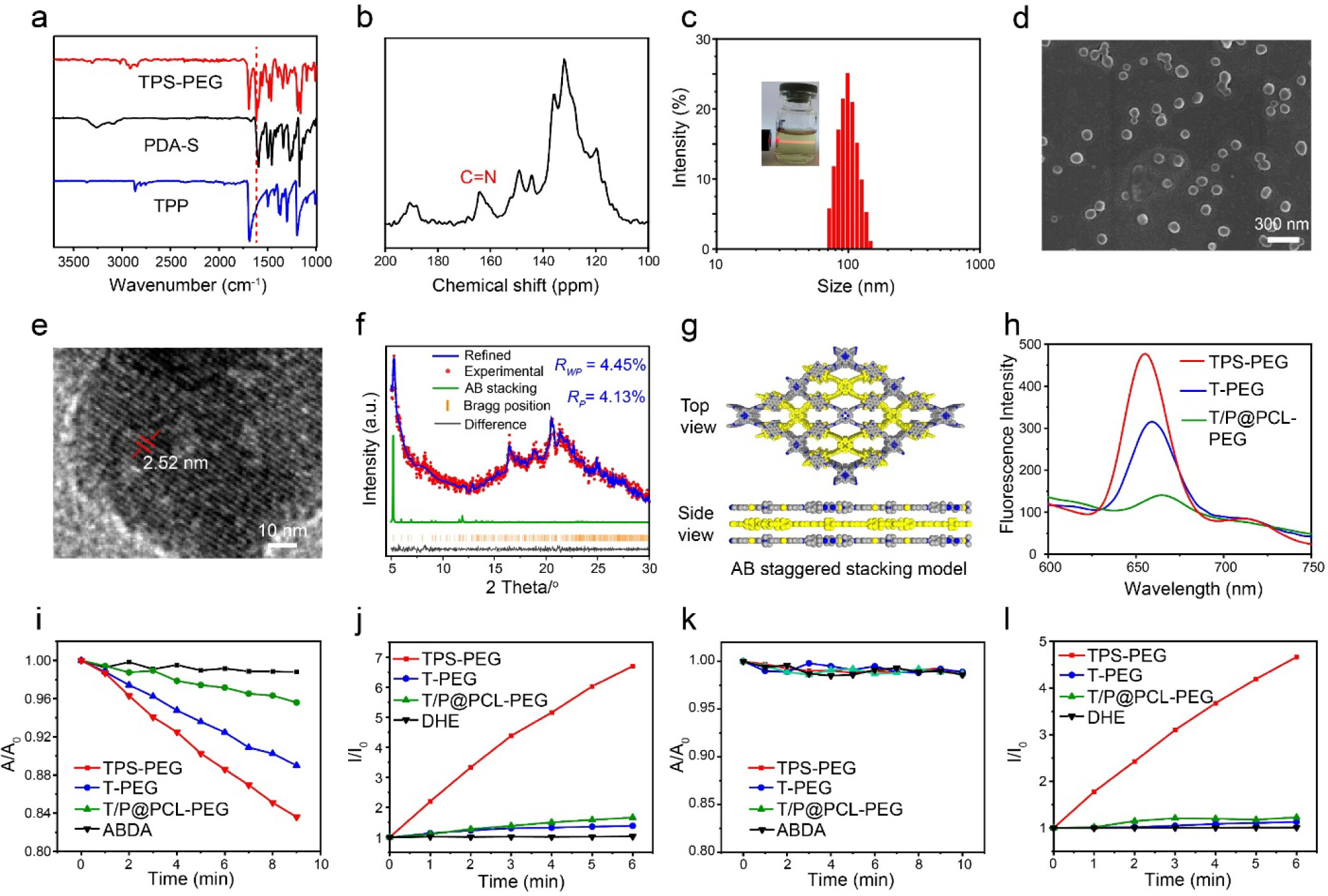
展望:
本文的研究为乏氧肿瘤的光动力免疫治疗提供了一种新的策略,未来的研究可以进一步探索COF纳米光敏剂在其他类型肿瘤中的应用,以及其在临床治疗中的潜力。此外,还可以研究不同结构的COF纳米光敏剂对ROS生成效率的影响,以及如何进一步优化其光物理和光化学性质,以提高治疗效果和减少副作用。
Potent Covalent Organic Framework Nanophotosensitizers with Staggered Type I/II
Motifs for Photodynamic Immunotherapy of Hypoxic Tumors
文章作者:Qinghao Zhou, Guopu Huang, Jiale Si, Youshen Wu, Shangbin Jin, Yuanyuan Ji, and Zhishen Ge*
DOI:10.1021/acsnano.4c14555
文章链接:https://pubs.acs.org/doi/10.1021/acsnano.4c14555
本文为科研用户原创分享上传用于学术宣传交流,具体内容请查阅上述论文,如有错误、侵权等请联系修改、删除。未经允许第三方不得复制转载。





